NC : 干预肥胖新机制,竟然隐藏在肠道里?还能调控炎症代谢
近年来,肥胖及其相关代谢紊乱已成为一个备受关注的问题。有研究表明,白细胞介素 (IL) 22 干预炎症和代谢紊乱,并在维持肠道内稳态方面发挥着至关重要的作用。IL-22 属于 IL-10 家族细胞因子,由 Th17 细胞和 3 型先天淋巴样细胞产生,通过其受体复合物 ( IL-22RA1 / IL-10Rβ ) 传递信号。但目前尚不清楚 IL-22 干预肥胖的肠道稳态的具体作用机制。
2024 年 2 月 21 日,美国石溪大学研究团队在 Nature Communications 杂志发表了题为 Intestinal IL-22RA1 signaling regulates intrinsic and systemic lipid and glucose metabolism to alleviate obesity-associated disorders 的文章,阐明了 IL-22RA1 信号传导在调控肠道菌群代谢和肥胖相关疾病糖脂代谢中的关键作用。

图片来源:Nature Communications
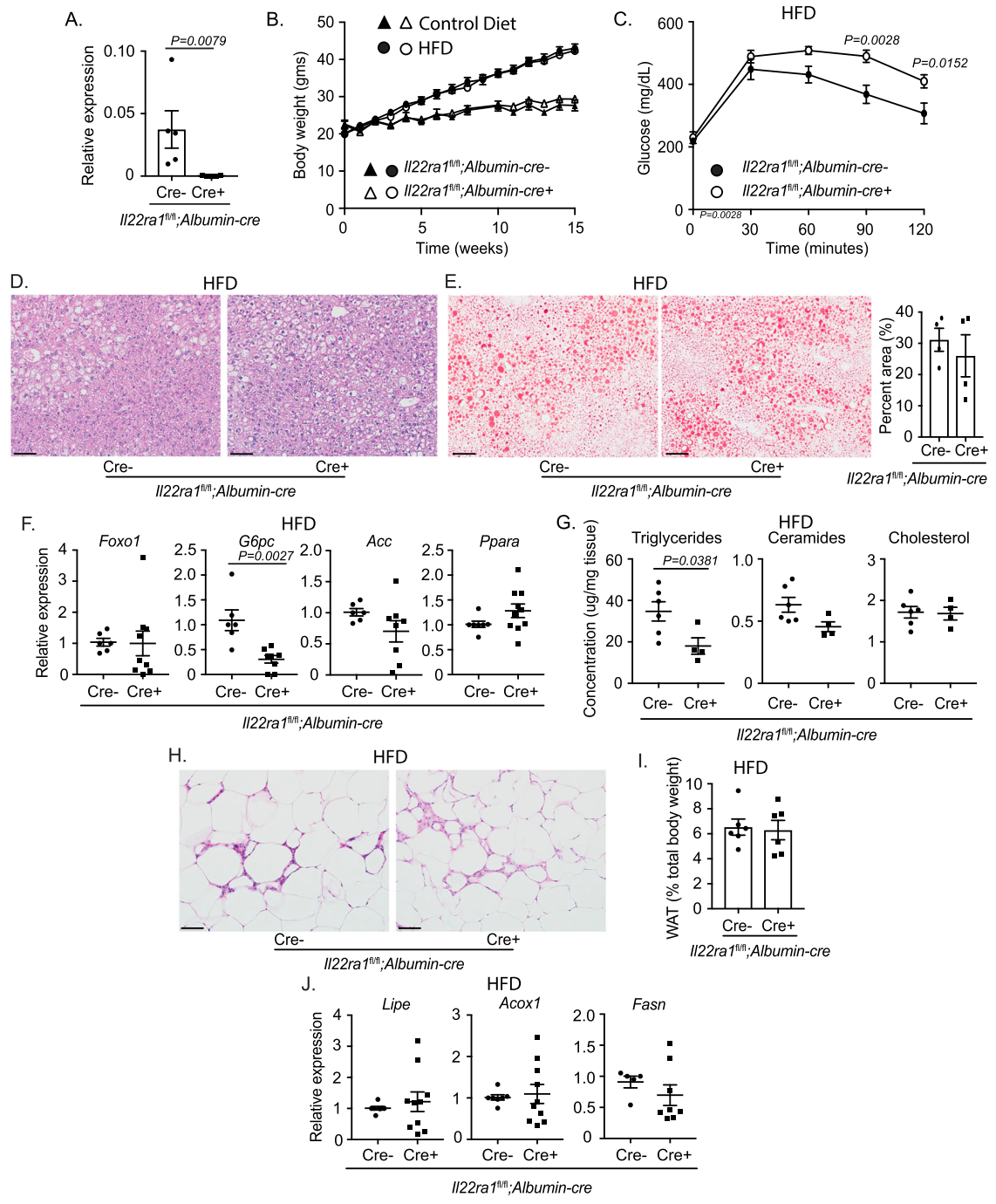
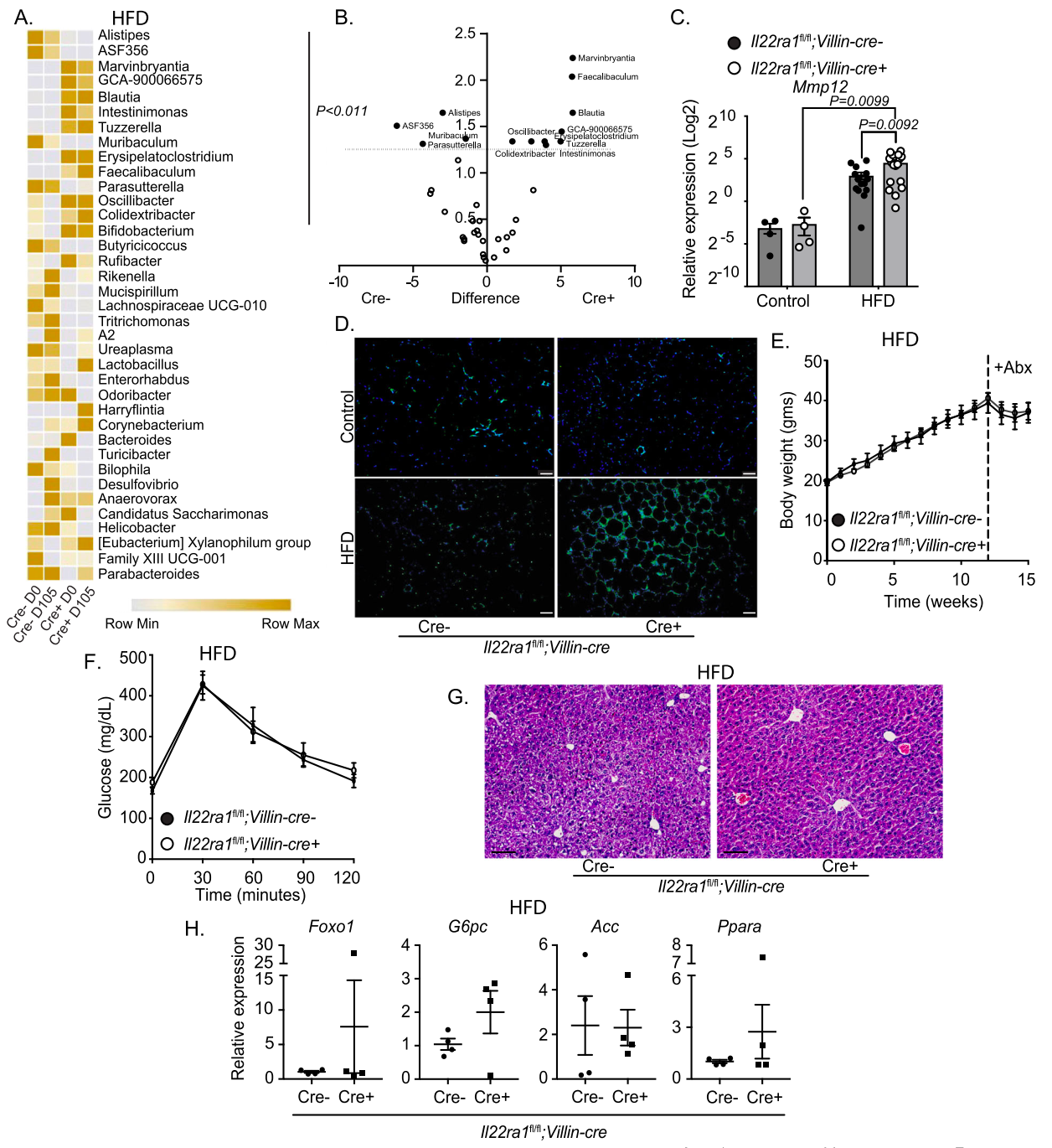
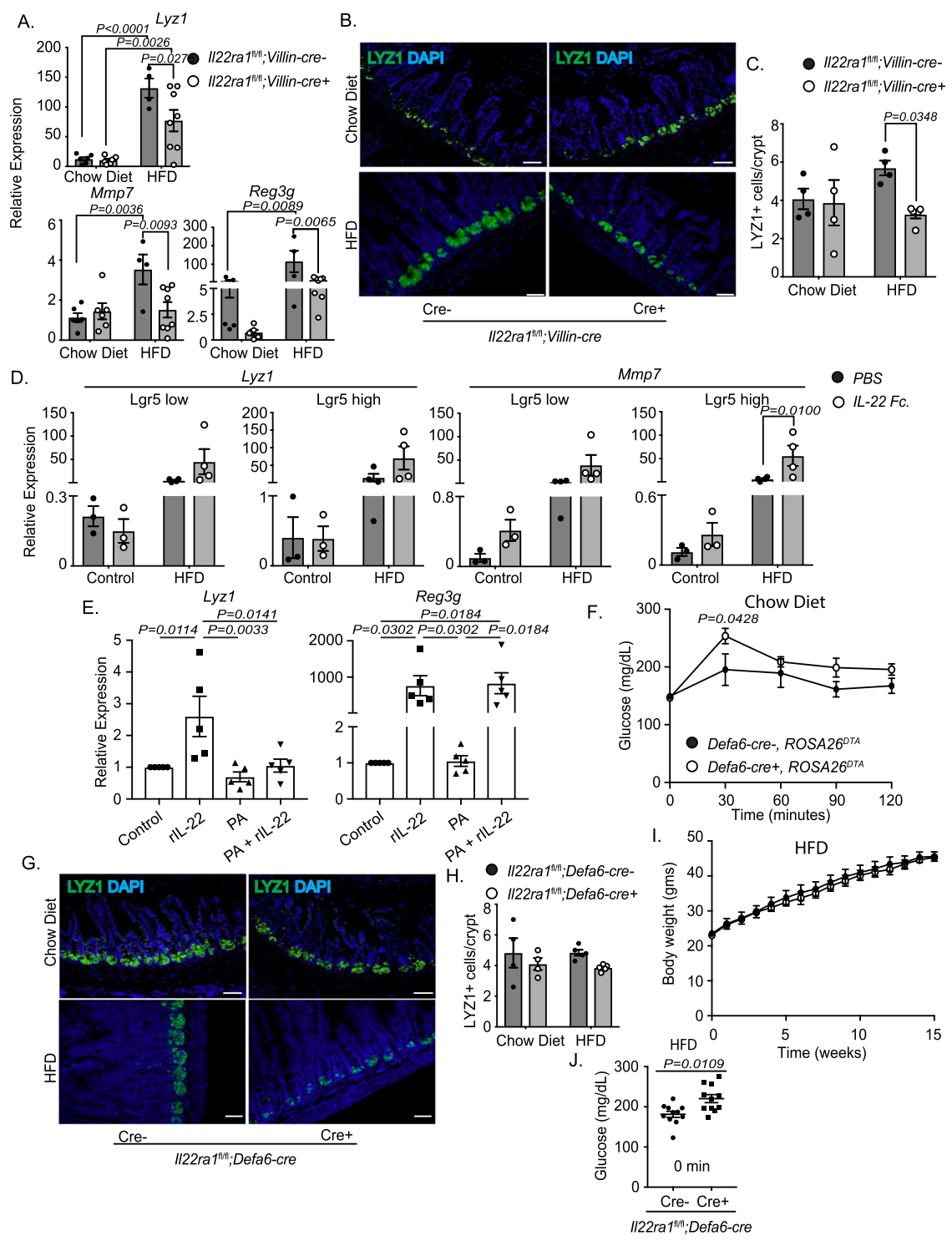
肠道上皮特异性 IL-22RA1 缺乏介导全身性代谢紊乱首先,研究员们探究了 IL-22 的代谢调控机制,发现 IL-22 在白色脂肪组织 (WAT)、肝脏和肠道脂质代谢调节中确实存在差异。为了研究 IL-22RA1 信号传导到特定组织的代谢机制,他们构建了肠上皮 Il22ra1 特异性敲除小鼠模型,经过高脂饮食 (HFD) 饲喂 16 周后,发现小鼠葡萄糖清除能力受损。然后,为了评估肠道 IL-22RA1 信号是否介导肠外代谢,他们将研究重点聚焦在肝脏,发现肠上皮 Il22ra1 特异性敲除小鼠伴有肝细胞球化和脂滴沉积增加。而且,经过葡萄糖和脂质代谢关键基因的分析,观察到小鼠该类基因转录水平显著降低,而总神经酰胺和胆固醇水平升高。表明肠道 IL-22RA1 信号在调节肠外基因表达、脂质代谢和沉积中起着重要作用。图片来源:Nature Communications肝脏特异性 IL-22RA1 缺乏会损害全身葡萄糖代谢为了进一步评估 IL-22RA1 信号在肝脏中的特异性机制,研究员们构建了肝脏 Il22ra1 特异性敲除小鼠,发现肝脏 Il22ra1 特异性敲除小鼠的葡萄糖清除率明显受损,说明肝脏 IL-22RA1 信号还调控全身葡萄糖代谢。接着,他们通过对 HFD 小鼠的肝脏组织进行气相色谱分析,进一步评估脂质代谢的变化,发现肝脏 Il22ra1 特异性敲除小鼠的甘油三酯水平显著降低,但神经酰胺和胆固醇水平相似。证实了组织特异性 IL-22RA1 信号在调控代谢中的诱导作用。图片来源:Nature Communications肠道 IL-22RA1 信号以菌群依赖方式介导肠外代谢接下来,研究员们评估了 IL-22 可能调控并介导全身代谢和炎症的肠道因子,并且探索了 IL-22 介导的菌群调节是否会影响 HFD 摄入后的全身代谢。通过双因素 (饮食、基因型) 分析,发现 13 个菌属存在显著差异,而且肠上皮 Il22ra1 特异性敲除小鼠的 Oscillibacter 属(之前有报道称该菌属会使葡萄糖代谢紊乱)丰度更高,表明肠道 IL-22RA1 信号对于调控全身代谢的菌群很重要。最后,为了进一步评估菌群的组成性差异是否会介导 HFD 摄入后的肠道外代谢和炎症反应,他们在 HFD 摄入最后 4 周后,通过广谱抗生素干预肠上皮 Il22ra1 特异性敲除小鼠来消耗菌群,结果发现差异性不大。图片来源:Nature Communications肠道 IL-22RA1 信号上调 Paneth 细胞数量和功能Paneth 细胞的主要作用是通过产生抗菌肽来调节肠道菌群。研究员们发现,HFD 摄入后,肠上皮 Il22ra1 特异性敲除小鼠的回肠组织中显示 Paneth 细胞相关抗菌基因的表达降低,并且 LYZ1 阳性细胞数量减少。表明肠道 IL-22RA1 信号通路介导了 HFD 后 Paneth 细胞的抗菌能力和数量。为了确定 Paneth 细胞数量是否直接介导了机体代谢,他们构建了 Paneth 细胞特异性敲除小鼠。通过糖耐量检测,发现 Paneth 细胞特异性敲除小鼠全身糖代谢受损。接下来,为了进一步阐明 IL-22RA1 信号在 Paneth 细胞中的作用,他们构建了 Paneth 细胞特异性 Il22ra1 敲除小鼠。发现 HFD 摄入后,Paneth 细胞特异性 Il22ra1 敲除小鼠的空腹血糖水平明显更高。因此,IL-22 可能作用于 Paneth 细胞,调节其功能,并在一定程度上维持 HFD 期间的基线葡萄糖代谢。本研究中,研究员们阐明了 IL-22RA1 信号在 HFD 介导的代谢紊乱中的组织特异性作用,以及在肠道、肝脏和脂肪组织代谢功能的差异性,强调了肠道 IL-22RA1 信号在调节肠道和肠外代谢以及影响这些结果的潜在免疫和菌群机制中的关键作用。1.Gaudino SJ, et al. Intestinal IL-22RA1 signaling regulates intrinsic and systemic lipid and glucose metabolism to alleviate obesity-associated disorders. Nat Commun. 2024 Feb 21;15(1):1597.2.Keir M, Yi Y, Lu T, Ghilardi N. The role of IL-22 in intestinal health and disease. J Exp Med. 2020 Feb 13;217(3):e20192195.3.Morigny P, et al. Lipid and glucose metabolism in white adipocytes: pathways, dysfunction and therapeutics. Nat Rev Endocrinol. 2021 May;17(5):276-295.