

1 月 28 日,北京大学詹启敏院士团队在期刊《Signal Transduction and Targeted Therapy》上发表了题为 AKT2S128/CCTαS315/319/323-positive cancer-associated fibroblasts (CAFs) mediate focal adhesion kinase (FAK) inhibitors resistance via secreting phosphatidylcholines (PCs) 的研究论文,研究人员发现磷脂酰胆碱(PCs)可能被用作食管鳞状细胞癌(ESCC)诊断的新生物标志物。这些数据为针对代谢物相关途径治疗 ESCC 提供了新的策略。

https://www.nature.com/articles/s41392-023-01728-6#Sec11
研究背景
食管鳞状细胞癌 (ESCC) 患者的预后很差,5 年生存率不到 15%。各种风险因素,如烟酒成瘾、遗传缺陷以及其他一些有害的环境因素都可能诱发 ESCC 的形成和发展。重要的是,细胞毒性、靶向和免疫治疗的疗效不足导致了生存率的下降。ESCC 的综合多组学分析将为探索新的诊断标志物和治疗靶点提供精确的分子分类,从而提高 ESCC 的治疗效果。相应地,探索信号成瘾、脆弱性或其他一些重要的肿瘤相关通路,并评估其靶向性和可药物性,可以为 ESCC 的精确治疗提供研究范式。
治疗耐药的关键机制是肿瘤微环境 (TME) 周围的 ESCC 细胞,特别是其主要成分-癌症相关成纤维细胞 (CAFs)。CAFs 在实体肿瘤的 TME 中发挥核心作用,诱导肿瘤的各种恶性表型,包括持续生长、侵袭转移、血管生成、上皮-间充质转化和肿瘤干细胞的形成。肿瘤细胞如何利用代谢营养物质及其影响的信号通路是重点研究的领域。为了应对 TME 带来的代谢挑战,肿瘤细胞和 CAFs 合作相互作用,促进肿瘤恶性发展。此外,CAFs 的代谢特征、CAFs 衍生的代谢产物如何作用于肿瘤恶性程度以及肿瘤细胞对治疗药物的反应仍不清楚。
研究进展
在本研究中,研究人员发现 FAK 抑制剂刺激 AKT2S128/ cct α s315 /319/323 阳性 CAFs 亚群分泌 PCs,从而诱导恶性细胞 STAT3 活化,进而促进肿瘤细胞的治疗抵抗。目前的数据确立了 CAFs -FAK 调节和代谢产物介导的肿瘤恶性控制与低基质 FAK 表达的人食管鳞癌相关的概念,并发现潜在的抗肿瘤治疗的新靶点。重要的是,研究人员发现血浆 PCs 可以作为食管鳞癌分期的生物标志物。
本研究还强调了高血浆 PCs 在促进肿瘤进展中的作用,并可能被开发为针对实体肿瘤的治疗靶点。越来越多的报告表明,代谢物与肿瘤的发展之间存在关系。根据本研究结果,研究人员推测 ESCC 患者血浆 PCs 的高浓度在 ESCC 恶性程度中起着至关重要的作用。抑制 PCs 对肿瘤细胞的作用可以有效地阻止肿瘤恶性进展。综上所述,血浆 PCs 水平不仅可以作为鉴别肿瘤分期的生物标志物,也可以作为肿瘤治疗的潜在靶点或增强靶向治疗的抗肿瘤疗效。
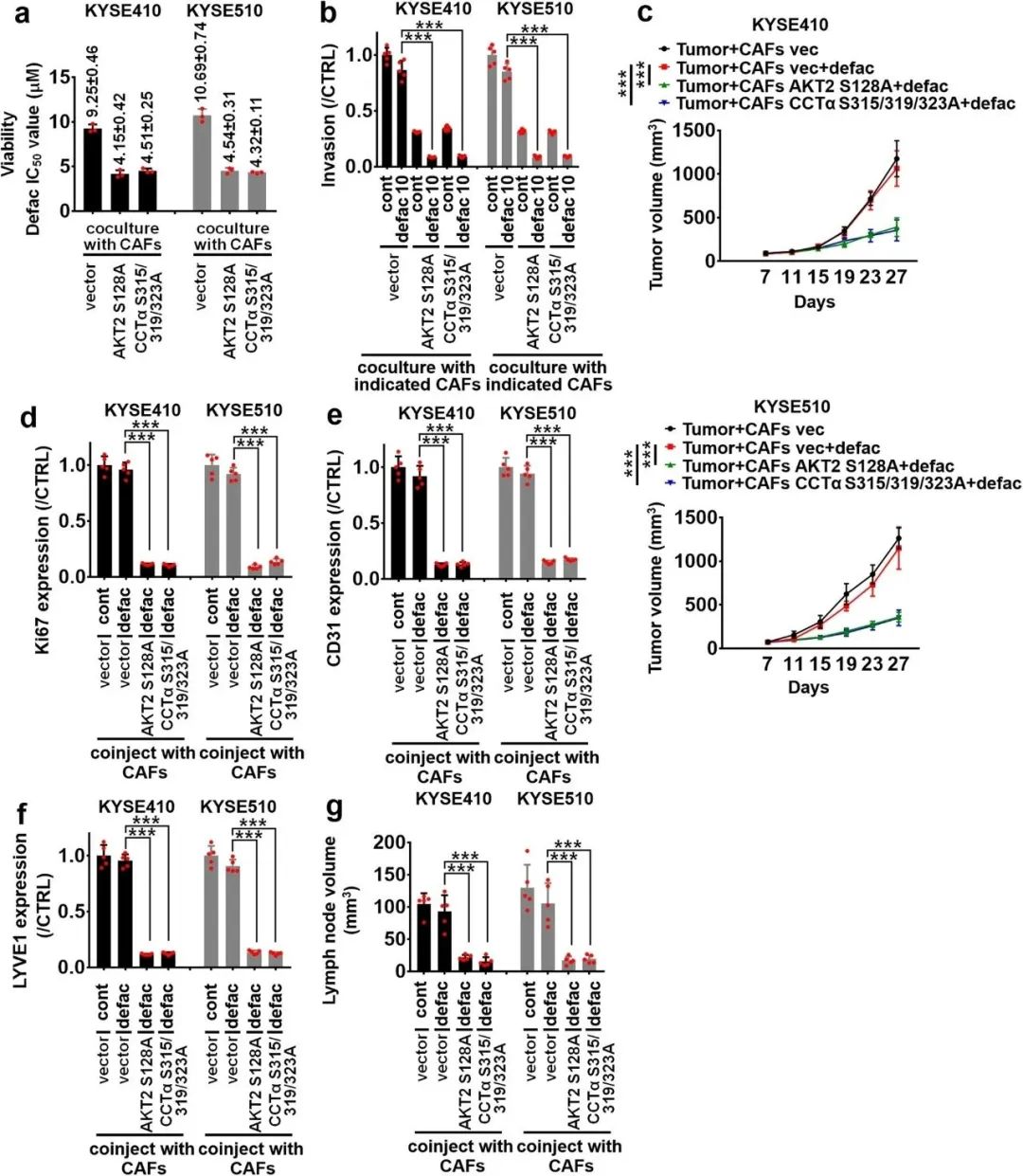
CAFs 衍生的 AKT2/CCTα 轴介导地法替尼在 ESCC 治疗中的耐药
研究结论
综上所述,结合多组学,研究人员系统地研究了基于 PCs 的 CAFs 和肿瘤细胞之间的旁分泌交流,以限制 FAK 抑制剂的抗肿瘤疗效。机制上,CAFs 衍生的 AKT2/CCTα 轴及其激活的肿瘤内 JAK2/STAT3 通路的改变诱导了 FAK 抑制剂在肿瘤治疗中的耐药。重要的是,PCs 有可能成为食管鳞癌诊断的新型生物标志物。这些数据为靶向代谢相关通路治疗食管鳞癌提供了新的策略。
参考资料:
https://www.nature.com/articles/s41392-023-01728-6#Sec11